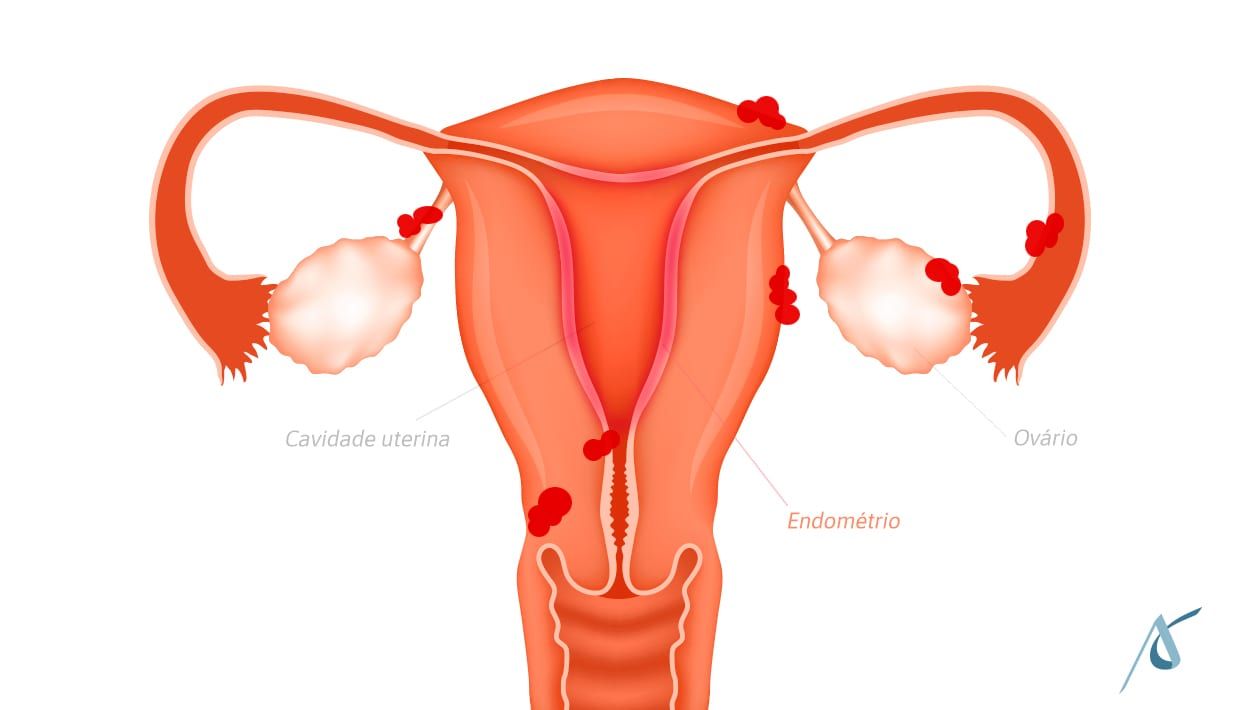
Uma das principais causas de infertilidade feminina, a endometriose tem como característica o crescimento de um tecido semelhante ao endométrio fora da cavidade uterina.
Endométrio é o tecido que reveste a cavidade uterina. A cada ciclo menstrual, seu crescimento e espessamento é estimulado pela ação hormonal, com o propósito de prepará-lo para receber o embrião. Ele vai nutri-lo e abrigá-lo até que a placenta seja formada.
O tecido endometrial ectópico, por outro lado, tende a se desenvolver frequentemente em órgãos como os ovários e tubas uterinas ou nos ligamentos que sustentam o útero, comprometendo a fertilidade.
Porém, também pode crescer em outras regiões da pelve e do abdômen e, em casos mais raros, nas membranas que revestem os pulmões e o coração.
O desenvolvimento do tecido provoca um processo inflamatório e diferentes sintomas, que se manifestam de acordo com o local de crescimento, profundidade ou grau de comprometimento dos órgãos atingidos.
No entanto, em muitos casos a endometriose é assintomática.
Este texto explica detalhadamente a endometriose, da classificação e sintomas provocados por cada tipo, ao diagnóstico e tratamentos indicados para cada caso.
Quais são as causas de endometriose?
Por ser uma doença crônica e inflamatória complexa, as causas que provocam a endometriose ainda permanecem desconhecidas. No entanto, diversas teorias surgiram para explicar o crescimento do tecido ectópico desde que a doença foi descrita pela primeira vez, ainda no século XIX, em 1860.
A mais aceita até hoje é a “teoria da implantação de Sampson”, proposta pelo ginecologista americano John Albertson Sampson no início do século XX.
De acordo com a observação de Sampson,
fragmentos do endométrio, geralmente eliminados pela menstruação, retornam pelas tubas uterinas e implantam em outros locais.
A teoria da metaplasia celômica também tem sido avaliada atualmente, principalmente por explicar a ocorrência de endometriose em regiões da cavidade abdominal e em meninas na pré-puberdade.
Essa teoria sugere que as células que originaram o endométrio e o tecido germinativo ovariano permanecem no peritônio (membrana que recobre a parede abdominal) e são transformadas em tecido ectópico pela ação de hormônios e por fatores imunológicos.
A ação hormonal também é apontada como possível causa,
uma vez que a incidência da doença é mais alta em mulheres na idade reprodutiva. A explicação é a de que o crescimento do tecido ectópico, assim como o endométrio, é estimulado por hormônios, como o estradiol e a progesterona.
Estudos mais recentes, por outro lado, sugerem, ainda, que a endometriose pode ser genética. A sugestão é justificada pelo alto número de registros da doença em parentes de primeiro grau das mulheres com a doença.
Alguns fatores também podem aumentar o risco para o desenvolvimento de endometriose. Mulheres que nunca tiveram filhos ou que foram mães após os 30 anos, por exemplo, têm risco aumentado. Outros fatores de risco incluem:
- Menstruação precoce;
- Menopausa tardia;
- Ciclos menstruais curtos (menos de 27 dias) ou períodos abundantes e de longa duração;
- Níveis altos de estrogênio;
- Anomalias uterinas;
- Obstruções que impedem a saída do fluxo menstrual;
- Peso abaixo do normal;
- Hábitos como alcoolismo.
A endometriose registra percentuais bastante significativos de infertilidade: cerca de 15% de mulheres em idade reprodutiva podem ser afetadas pela doença e até 50% delas podem ter infertilidade.
Entenda como a endometriose é classificada
A classificação da endometriose considera critérios como a localização das lesões, quantidade e profundidade, comprometimento dos órgãos, presença e número de endometriomas ovarianos, um subtipo da doença.
O sistema de classificação é aceito internacionalmente e foi proposto pela Sociedade Americana de Medicina Reprodutiva (ASRM): mínima (estágio I), leve (estágio II), moderada (estágio III) ou grave (estágio IV).
- Estágio 1 (doença mínima): implantes isolados e sem aderências significativas;
- Estágio 2 (doença leve): implantes superficiais com menos de 5 cm, sem aderências significativas;
- Estágio 3 (doença moderada): múltiplos implantes, aderências peritubárias e periovarianas evidentes;
- Estágio 4 (doença grave): múltiplos implantes superficiais e profundos, incluindo endometriomas, aderências densas e firmes.
Além dos estágios de desenvolvimento, a endometriose é ainda morfologicamente classificada em três subtipos:
Endometriose peritoneal superficial: nos estágios I e II de desenvolvimento, a endometriose peritoneal tem como principal característica a formação de pequenas lesões, geralmente planas e rasa e localizadas no peritônio.
É um tipo menos agressivo da doença, pois as lesões ainda não invadiram outros órgãos.
No entanto, algumas pacientes apresentam sintomas importantes mesmo na endometriose superficial, que deve ser constantemente observada para evitar que ocorra uma evolução.
Endometriose ovariana: a presença de endometriomas ovarianos, um tipo de cisto preenchido por líquido de aspecto achocolatado, caracteriza a endometriose ovariana. Eles tendem a apresentar diferentes tamanhos e são bastante comuns em mulheres com a doença.
Endometriose infiltrativa profunda: no estágio IV de desenvolvimento, nesse tipo de endometriose as lesões são mais profundas e já invadiram o peritônio e locais como a região retrocervical (atrás do colo uterino), o septo retovaginal (entre reto e vagina), a vagina, o intestino, as paredes da bexiga e ureteres.
Porém, a classificação da endometriose permanece controversa, principalmente pela diversidade de suas manifestações, mesmo que o sistema proposto pela ASRM seja bastante útil na orientação do tratamento pós-cirúrgico, especialmente quando a doença causa infertilidade.
Em 2014, a Sociedade Mundial de Endometriose organizou um evento global com a participação de especialistas de 29 países. Na ocasião, foi recomendada a incorporação de dois outros sistemas de classificação às diretrizes da ASRM para todas as mulheres que forem submetidas à cirurgia de extração do tecido ectópico:
O Enzian-Score, que classifica a endometriose profunda a partir do envolvimento de outros órgãos, determinando a severidade e disseminação da doença;
O EFI, um sistema de pontuação que considera diferentes fatores relacionados à infertilidade.
Quais são os sintomas de endometriose?
Na maioria das vezes, os sintomas de endometriose ocorrem de acordo com o local de crescimento, profundidade e grau de comprometimento dos órgãos atingidos. No entanto, essa correlação nem sempre é clara. Os mais frequentemente manifestados incluem:
- Dismenorreia – também conhecida como cólica menstrual, a dismenorreia é o principal sintoma manifestado por pacientes com endometriose, com uma prevalência estimada em 62,2%, geralmente é mais intensa durante o período menstrual.
- Dor pélvica crônica ou acíclica – durante o ciclo menstrual pode ainda ocorrer dor na região pélvica, que se manifesta repentinamente ou de forma intermitente. Além do desconforto, ela pode ser pulsante, aguda e frequentemente piora no decorrer do tempo.
- Dispareunia – quando há dor durante as relações sexuais a condição é conhecida como dispareunia. Em mulheres com endometriose, é mais frequente quando o tecido ectópico provoca lesões profundas na vagina e ligamentos uterossacros, que ligam o útero à coluna e são um local comum de desenvolvimento do tecido ectópico.
- Alterações urinárias – alterações urinárias normalmente estão relacionadas ao tamanho das lesões que se desenvolvem na bexiga e à intensidade do problema. Disúria (dificuldade para urinar acompanhada de dor), hematúria (presença de sangue na urina), polaciúria (micção anormal e frequente) e urgência miccional, são os sintomas mais observados.
- Alterações intestinais – alterações no hábito intestinal com distensão abdominal, caracterizadas por sangramento nas fezes, constipação, disquezia (dor ou dificuldade em evacuar) e dor anal, tendem, ao mesmo tempo, a ocorrer de forma cíclica durante o período menstrual.
Embora sejam menos comuns, outros sintomas podem ainda se manifestar durante o período menstrual. Geralmente também são cíclicos e surgem como consequência de lesões em localizações menos usuais.
Entre eles estão dor irradiada para membros inferiores, vulvodínea (dor em torno da abertura da vagina), dor na região glútea, dor torácica, hemoptise (expectoração de sangue) e dor epigástrica.
Nem sempre os sintomas se manifestam da mesma forma nas portadoras de endometriose.
A variação da percepção de dor, por exemplo, está relacionada a diversos fatores (psicológicos, ambientais, comportamentais), por isso a intensidade pode ser diferente entre pacientes com o mesmo grau da doença.
Como a endometriose é diagnosticada?
O diagnóstico se baseia nos mesmos critérios de classificação: localização, quantidade e profundidade, além da presença de endometriomas ovarianos.
Para determinar a localização das lesões, são realizados exames de imagem, como a ultrassonografia transvaginal e pélvica e ressonância magnética (RM), ambos com preparo intestinal.
As chances de gravidez, por outro lado, são determinadas a partir do grau de comprometimento, idade da mulher, tempo de infertilidade, gravidez anterior e funcionamento dos órgãos reprodutores.
O tratamento é indicado de acordo com cada caso, baseado nos resultados diagnósticos.
Quais são os tratamentos indicados para endometriose
O tratamento para endometriose é individualizado, determinado de acordo com a intensidade da dor manifestada e o desejo de engravidar no momento.
Para pacientes que manifestam dor e não pretendem engravidar, geralmente são prescritos contraceptivos (orais, DIU, anel ou injetável) combinados ou somente com progesterona.
Se não houver melhora, a recomendação passa a ser cirúrgica. A cirurgia é realizada por videolaparoscopia e também é o tratamento indicado para mulheres com dor severa e infertilidade.
O percentual de gravidez natural é bastante expressivo após a remoção do tecido endometrial ectópico.
Por outro lado, nos casos em que há infertilidade sem a manifestação de dor, as técnicas de reprodução assistida são a principal indicação.
A relação sexual programada (RSP) e a inseminação intrauterina (IIU), de baixa complexidade, são recomendadas para mulheres com endometriose mínima ou leve, ainda nos estágios iniciais.
Na RSP, no entanto, as tubas uterinas e espermatozoides devem estar saudáveis, pois a fecundação ocorre de forma natural.
Já a IIU possibilita também o tratamento quando há pequenas alterações nos espermatozoides, pois eles são selecionados com o auxílio de técnicas de preparo seminal, e os melhores são depositados no útero durante o período fértil.
A fertilização in vitro (FIV), de alta complexidade, é indicada quando a endometriose é moderada ou grave, para endometriose ovariana ou se não houver sucesso nos tratamentos anteriores.
Mesmo que todas as técnicas proporcionem o sucesso da gravidez, a FIV apresenta os percentuais mais expressivos por ciclo de realização.
A indicação do tratamento, além de individualizada, deve ser discutida com o médico, levando em consideração riscos e benefícios de cada abordagem.